転移性脳腫瘍
肺がんなどの癌腫が他臓器に転移した場合の治療法は、抗がん剤が主に用いられますが、脳に転移した場合(転移性脳腫瘍)は、抗がん剤の効果が小さいため、また別の治療法を検討する必要があります。近年は癌に対する化学療法などの治療成績が向上し、転移性脳腫瘍の患者さんの数は増加する傾向にあります。
従来、転移性脳腫瘍に対する標準的治療は、手術 + 全脳照射 とされていましたが、全脳照射による高次脳機能障害を避ける目的で、ガンマナイフが積極的に用いられるようになっています。当院では、転移性脳腫瘍に対してガンマナイフ治療を行い非常に良好な成績を得ています。この治療は身体の負担が少なく、短期間で終わり、高い有効性を持つために転移性脳腫瘍の患者さんに対して勧められる治療と考えます。
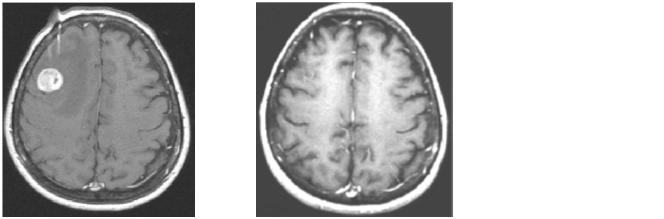
(左)右前頭葉に肺がんの脳転移が認められる。(右)ガンマナイフ治療後6ヶ月経過し、転移性脳腫瘍が完全に消失している。
関連記事
-
 形成外科脳神経外科動静脈奇形動静脈奇形は動静脈シャント疾患で,頭頚部,体幹,四肢など様々な部位に発生します.症状は部位によって違いもありますが,共通しているのが最初は皮膚の発赤・熱感のみ (静止期)であったものが,次第に病変部が腫脹して血管の拍動を認めるようになり (拡張期),さらに進行すると病変部の皮膚に潰瘍ができ,出血するようになります (破壊期).症状は動静脈シャントの血流量と比例しており,その血流量は年齢が上がるにつれて増えてくることが多く,また外傷,感染,ホルモン変化,血行動態の変化などによって急激に増えることもあります. 治療のタイミングは患者さん毎に検討する必要がありますが,疼痛,潰瘍,出血などの症状が出現している場合や美容的理由がある場合には治療適応となります.病変部の発赤や腫脹のみの場合には病変の大きさや血管構築などから根治が可能かどうかで治療適応を判断します. 症状,治療のタイミングともに病変の部位で大きな違いはないので,頭頚部動静脈奇形も参照してください. 治療には血管内治療や外科手術(切除+再建)がありますが,その複雑な血管構築からほとんどの場合で血管内治療と外科手術を組み合わせて行います.血管内治療は病変がどの部位でも脳神経外科で行いますが,外科手術は病変の部位に応じて担当科は変わります.病変の範囲が限られたものでは根治が見込めますが,広範囲なものは根治が困難であるのが現状です.詳しく見る
形成外科脳神経外科動静脈奇形動静脈奇形は動静脈シャント疾患で,頭頚部,体幹,四肢など様々な部位に発生します.症状は部位によって違いもありますが,共通しているのが最初は皮膚の発赤・熱感のみ (静止期)であったものが,次第に病変部が腫脹して血管の拍動を認めるようになり (拡張期),さらに進行すると病変部の皮膚に潰瘍ができ,出血するようになります (破壊期).症状は動静脈シャントの血流量と比例しており,その血流量は年齢が上がるにつれて増えてくることが多く,また外傷,感染,ホルモン変化,血行動態の変化などによって急激に増えることもあります. 治療のタイミングは患者さん毎に検討する必要がありますが,疼痛,潰瘍,出血などの症状が出現している場合や美容的理由がある場合には治療適応となります.病変部の発赤や腫脹のみの場合には病変の大きさや血管構築などから根治が可能かどうかで治療適応を判断します. 症状,治療のタイミングともに病変の部位で大きな違いはないので,頭頚部動静脈奇形も参照してください. 治療には血管内治療や外科手術(切除+再建)がありますが,その複雑な血管構築からほとんどの場合で血管内治療と外科手術を組み合わせて行います.血管内治療は病変がどの部位でも脳神経外科で行いますが,外科手術は病変の部位に応じて担当科は変わります.病変の範囲が限られたものでは根治が見込めますが,広範囲なものは根治が困難であるのが現状です.詳しく見る -
 脳神経外科動静脈シャント疾患 (動静脈奇形、動静脈瘻)1. 動静脈シャント疾患とは 血液は正常では動脈-細動脈-毛細血管-細静脈-静脈の順に流れています (図1A).一方,動静脈シャント (短絡)は動脈が毛細血管を介さずに静脈が直接つながってしまった状態です.動静脈シャントを認める血管奇形の総称を動静脈シャント疾患と言い,動静脈奇形や動静脈瘻が含まれます. 毛細血管には様々な役割がありますが,その1つに血圧の調整があります.したがって毛細血管を介さない動静脈シャント疾患では,圧の高い動脈の血流が,本来は圧の低い静脈に直接流れ込んでしまうため病変部に負担がかかり,その結果として様々な症状を引き起こします. 動静脈奇形は比較的細い動静脈レベルで動静脈シャントが形成されており,動静脈シャント部はナイダスと呼ばれる異常血管の塊となっています (図1B).一方,動静脈瘻は動静脈奇形よりも太いレベルで動静脈シャントが形成されており,多くの場合,動静脈シャント部の静脈が拡張して静脈瘤となっています (図1C).動静脈シャントができる原因は完全には解明されていませんが,遺伝子異常,炎症,外傷 (手術を含む)などが原因の1つと考えられています. 図1A 図1B 図1C 図1A:正常の血管構造 血管は動脈,細動脈,毛細血管の順にその径が小さくなり,血管にかかる圧は主に細動脈と毛細血管レベルで下がっていく.その後,細静脈,静脈の順にその径は太くなるが,血管にかかる圧は低いままである. 図1B:動静脈奇形 動静脈奇形は比較的細い動脈と静脈がナイダスと呼ばれる異常血管の塊を介して動静脈シャントを形成している. 図1C:動静脈瘻 動静脈瘻は動静脈奇形よりも太いレベルで動脈と静脈が直接つながっており,動静脈シャント部には負担がかかるため静脈瘤を形成している. 動静脈シャント疾患は病変の部位,血管の構造,血流の速さ (シャント血流量)などの個人差が非常に大きく,そのため症状や適切な治療法は患者さん毎に異なります.また頚部内頚動脈狭窄症や脳動脈瘤よりも稀な疾患で,治療もより戦略的に行う必要があり,専門性の高い疾患となります.安易に治療をすることで,その先の治療が困難になることもありますので,最初から専門施設での治療をお勧めします. 動静脈シャント疾患は脳や脊髄だけでなく顔面,手足,肺など全身のどこにでもできる可能性があります.当院では脳・脊髄に限らず全身のあらゆる動静脈シャント疾患に対して脳神経外科が対応しています.以下に代表的な動静脈シャント疾患である脳動静脈奇形,硬膜動静脈瘻,脊髄・脊椎動静脈シャント疾患,頭頚部動静脈奇形,肺動静脈瘻について解説していきます. 2. 脳動静脈奇形 脳の中にできた動静脈奇形 (図2A)で,多くは20~40歳代に脳出血で発症します.また出血以外にも頭痛やけいれんなどで発症することもあります.脳出血で発症した場合には病変の部位によって運動麻痺,言語障害などの様々な神経症状をきたし,これらは後遺症となるリスクがあります.さらに出血が大きい場合には生命が脅かされることもあります. 図2A 図2A:脳動静脈奇形の血管構造 正常の脳動脈からナイダスへの栄養動脈が分岐し,動静脈シャントの血流はナイダスから流出静脈へと向かう. ナイダス部の脳は機能していないが,その周囲の脳は機能している. 年間出血率は2%前後ですが,脳動静脈奇形は見つかれば全例で治療すべきというわけではありません.経過観察での出血リスクと治療に伴う合併症のリスクとのバランスを考えて,患者さん毎に治療方針を決定します.治療には開頭手術,定位放射線治療 (ガンマナイフ),血管内治療などがありますが,その選択は患者さんの年齢,症状,病変の大きさ,血管構築などから総合的に判断します.具体的には脳ドックなどで偶然に見つかった場合 (無症状)には,経過観察か治療を行うにしてもリスクが低い定位放射線治療 (ガンマナイフ) (図2B)となります.出血以外の症状 (頭痛やけいれん)で見つかった場合 (非出血例)は,まず症状に対する対症療法 (内科的治療)を行いますが,そちらに抵抗性の場合には治療を検討します. 図2B 図2B:脳動静脈奇形に対するガンマナイフ 約200本のガンマ線 (放射線の1種)をナイダスに集中するように照射する. 1本1本のガンマ線は弱い放射線であるので,周囲の正常脳への影響は最小限であるが,ガンマ線が集まるナイダスには強い放射線が当たることになる. ガンマナイフでは治療後に病変はすぐに消失せず,2~3年かけて徐々に閉塞していく. 出血で発症した場合 (出血例)には再出血のリスクが高まりますので,全例で治療を行います.治療に関しては血管内治療 (術前塞栓術)を併用した開頭手術 (図2C, D)をまず検討し,開頭手術のリスクが高い部位の病変に対しては定位放射線治療をお勧めしています.また出血した部位がはっきりしている場合には,先に出血した部分のみを先に血管内治療で閉塞させ,その後に次の治療を検討することもあります.脳動静脈奇形は細い動静脈レベルで動静脈シャントが形成されていますので,血管内治療のみで安全かつ確実に根治させることは困難なのが現状です. 当院では出血例にせよ非出血例にせよ,より確実にまた安全かつ低侵襲に行える治療法を選択します. 図2C 図2D 図2C:脳動静脈奇形に対する血管内治療 (術前塞栓術) 太ももまたは手首から細いカテーテル (マイクロカテーテル)を栄養動脈まで誘導し,そこから血管を閉塞させるための液体 (液体塞栓物質)を注入する.正常の動脈は閉塞させない範囲で可能な限りナイダスを閉塞させ,開頭手術の際の出血が減るようにする. 図2D:脳動静脈奇形に対する開頭手術 開頭手術では丁寧にナイダスの部分のみを切除して,ナイダス周囲の正常脳や正常の血管を損傷しないようにする. 3. 硬膜動静脈瘻 硬膜は脳と頭蓋骨の間にある硬い膜で,脳を保護しているだけでなく,その中には正常の脳静脈が脳の表面から心臓へ還るための流出路である硬膜静脈洞も存在しています (図3A, B).硬膜動静脈瘻の多くはその硬膜静脈洞の壁またはその周囲に発生します.好発年齢は中高年代で,特に目の奥 (海綿静脈洞部)や耳の後ろ(横・S状静脈洞部)が好発部位となります.硬膜には非常に多くの動脈があるため,硬膜動静脈瘻は多数の栄養動脈が関与しているのが特徴です.また病変周囲の硬膜静脈洞が閉塞していることもあり,これは硬膜動静脈瘻による症状にも関係します. 図3A 図3B 図3A:硬膜と脳,頭蓋骨との関係 (断面図) 硬膜は脳と頭蓋骨との間にあり,その中には脳の表面からの静脈を受ける硬膜静脈洞が存在する. 図3B:代表的な硬膜静脈洞 (側面から見た図) 硬膜静脈洞は様々な部位で脳からの静脈を受けており,その血流を心臓へ還している. 硬膜動静脈瘻の症状は病変の部位により様々ですが,大きくは正常の脳静脈の流出を邪魔しているかどうかで分けられます.正常の脳静脈の流出を邪魔していないもの (図3C)の多くは,頭痛や心臓の拍動に一致した耳鳴りなどで発症し,症状の程度は個人差がありますが,脳うっ血や脳出血を起こすことはありません.したがって正常の脳静脈の流出を邪魔していない硬膜動静脈瘻は,症状の程度によって治療を行うか経過観察かを決定します.症状が軽く経過観察とした場合でも,後に脳静脈の流出を邪魔するようものへと進行することがあるため,定期的なMRI検査は必須となります. 図3C 図3C:硬膜動静脈瘻 (正常の脳静脈の流出を邪魔していないタイプ) 多数の栄養動脈がシャント部 (☆)に収束している. 動静脈シャントの異常血流はそこから硬膜静脈洞を使って心臓に向かって流出している. 一方,正常の脳静脈の流出を邪魔しているものは,病変周囲の硬膜静脈洞が閉塞している場合などで認められます (図3D).このような場合では動静脈シャントの異常血流が脳静脈に逆流することがあり,そうなると正常の脳静脈の流出は邪魔され,進行すると脳はうっ血して正常に機能しなくなります.そのためけいれんや運動麻痺,言語障害などの神経症状を認め,また認知障害が急速に進行することもあります.脳うっ血を起こしていると脳出血を起こすリスクも高く,年間出血率は8-19%になります.したがって正常の脳静脈の流出を邪魔している硬膜動静脈瘻は,症状がなくても基本的に治療をお勧めしています. 図3D 図3D:硬膜動静脈瘻 (正常の脳静脈の流出を邪魔しているタイプ) 硬膜静脈洞が閉塞していることで,動静脈シャントの異常血流は心臓側へ流出することができず,脳静脈を逆流して脳内へ向かっている. 硬膜動静脈瘻の治療のほとんどは血管内治療で行い,シャント部を閉塞させます.病変の部位,血管構築に応じて,動脈側からの治療 (経動脈的塞栓術) (図3E)もしくは静脈側からの治療 (経静脈的塞栓術) (図3F)を選択します.血管構築が複雑な場合は複数回の血管内治療を要することがあり,血管内治療で病変を消失させることが困難な場合には定位放射線治療 (ガンマナイフ)を追加することもあります.また血管内治療でカテーテルが到達困難な病変や脳神経麻痺が出現するリスクが高い病変などは開頭手術をお勧めすることもあります. 図3E 図3F 図3E:硬膜動静脈瘻に対する経動脈的塞栓術 太ももまたは手首から細いカテーテル (マイクロカテーテル)をできる限り栄養動脈の奥 (動静脈シャント部の近く)に誘導し,そこから血管を閉塞させる液体 (液体塞栓物質)を注入する.病変が消失することで動静脈シャントの異常血流が逆流していた脳静脈は正常の流れに戻る. 図3F:硬膜動静脈瘻に対する経静脈的塞栓術 太ももまたは首の静脈からマイクロカテーテルを病変に関与している硬膜静脈洞まで進め,動静脈シャントの異常血流が流出している硬膜静脈洞をシャント部も含めてプラチナコイルなどで閉塞させる.病変が消失することで動静脈シャントの異常血流が逆流していた脳静脈は正常の流れに戻る. 4. 脊髄・脊椎動静脈シャント疾患 脳から腰に向かって連続している脊髄は,その周囲を脳と同様に硬膜に覆われ,さらにその外側には骨である脊椎がある.また硬膜と脊椎の間には硬膜外腔というスペースが存在しており (図4A, B),その中を脊髄や脊椎に向かう動脈,脊髄からの神経,脊髄や脊椎からの静脈が走行しています.脊髄・脊椎動静脈シャント疾患には病変の部位に応じて,脊髄髄内動静脈奇形,脊髄辺縁動静脈瘻,脊髄硬膜動静脈瘻,脊髄硬膜外動静脈瘻などがある.脊髄・脊椎動静脈シャント疾患は脳の動静脈シャント疾患と比べて頻度はさらに低く,より専門性が高くなるので,その治療は経験豊富な施設で受ける必要があります. 図4A 図4B 図4A, B:正常の脊髄,硬膜,硬膜外腔,脊椎の位置関係 (A: 前方から見た図,B: 図4Aの①レベルでの横断面) 脊髄は脊椎の真ん中にあるトンネル状の空間 (脊柱管)に首から腰に向かって認められ,その周囲は硬膜に覆われている.硬膜と脊柱管の壁との間のスペースが硬膜外腔となる. 4-1. 脊髄髄内動静脈奇形 脊髄髄内動静脈奇形は脊髄内にできた動静脈奇形 (図4C)です.脊髄は部位によって頚髄 (首の高さ),胸髄 (胸の高さ),腰髄 (腰の高さ)に分けられます.その中で脊髄髄内動静脈奇形は胸髄レベルにできることが多く,20~40歳代に出血や脊髄うっ血 (脊髄の正常静脈の流れが邪魔されて脊髄が腫れる)などで発症することが多いのが特徴です.症状は病変に部位によって異なり,胸髄と腰髄レベルでは両下肢の運動麻痺,感覚障害,排尿・排便障害をきたし,頚髄レベルではそれらに加えて両上肢の運動麻痺,感覚障害や重症の場合には呼吸障害をきたします.年間出血率は4%前後で,約30%に動脈瘤を合併します. 図4C 図4C:脊髄髄内動静脈奇形 正常の脊髄動脈から複数の栄養動脈がナイダスへ分岐しており,動静脈シャントの異常血流はナイダスから流出静脈へ向かっている. ナイダス内に出血の原因となる動脈瘤を伴うことがある. 脊髄は脳と比べて非常に小さく,そのため外科手術,血管内治療ともに脳動静脈奇形よりもリスクが高くなるため,治療は原則的に症状を呈している場合にのみ行います.外科手術は根治できる可能性があるものの,手術の際に病変の周囲にある正常の脊髄が傷ついて神経症状が悪化する可能性もあるため,当院では外科手術よりも血管内治療を優先しています.血管内治療も目標は病変の消失ではなく,出血した動脈瘤部分のみを閉塞させるか (図4D),または安全なところのみ閉塞させて動静脈シャント量を減弱させ,再出血の予防または症状の改善を狙います. 図4D 図4D:脊髄髄内動静脈奇形に対する血管内治療 (経動脈的塞栓術) 太ももから細いカテーテル (マイクロカテーテル)を栄養動脈まで誘導し,そこから血管を閉塞させる液体 (液体塞栓物質)を注入する. 出血の原因となるナイダス内の動脈瘤を閉塞させることで,再出血の危険性を下げることができる. 4-2. 脊髄辺縁動静脈瘻 脊髄表面にできた動静脈瘻 (図4E)で,胸髄レベルにでき,動静脈シャント部には静脈瘤を認めることが多いのが特徴です.好発年齢は小児から若年者で,脊髄うっ血や出血だけでなく,静脈瘤が脊髄を圧迫して症状を呈することもあります.非常に稀な疾患なので年間出血率などの詳細は分かっていません.症状に関しては脊髄髄内動静脈奇形と同様ですが,病変の血管構築によっては治療で根治が期待できることが大きく異なります.脊髄辺縁動静脈瘻は脊髄の表面に存在するため外科手術も可能ですが,当院ではより低侵襲に行うことのできる血管内治療を選択しています (図4F).症状を認めている場合は全例で治療を行いますが,症状を認めていない場合 (無症状)でも一旦症状が出現すると後遺症となる危険性が高い疾患なので,治療のリスクとのバランスを見て治療をお勧めすることもあります. 図4E 図4F 図4E:脊髄辺縁動静脈瘻 脊髄辺縁動静脈瘻は脊髄の表面に存在し,脊髄髄内動静脈奇形よりも栄養動脈が太い.また動静脈シャント部には静脈瘤を伴うことが多い. 図4F:脊髄辺縁動静脈瘻に対する血管内治療 (経動脈的塞栓術) 太ももから細いカテーテル (マイクロカテーテル)を栄養動脈まで誘導する.そこから血管を閉塞させる液体 (液体塞栓物質)を注入して,動静脈シャントの異常血流を遮断する. 4-3. 脊髄硬膜動静脈瘻 脊髄を覆う硬膜にできた動静脈瘻 (図4G)で,中高年の男性に多く認められます.背骨で言うと肋骨がつながっている胸椎レベルに多く見られ,動静脈シャントの異常血流が脊髄の静脈に逆流することで脊髄の正常静脈の流れが邪魔されて脊髄がうっ血し,両下肢の運動麻痺,感覚障害,排尿・排便障害などで発症します. 図4G 図4G:脊髄硬膜動静脈瘻 脊髄硬膜動静脈瘻は脊髄を覆う硬膜に動静脈シャントを形成している. 動静脈シャントの異常血流が脊髄の静脈へ逆流することで,正常の脊髄静脈の流れを邪魔して脊髄うっ血をきたす. 治療は血管内治療と外科手術のどちらでも可能ですが,当院ではほとんどが血管内治療で行っています (図4H).ただし閉塞させる動脈の傍から脊髄への正常の枝がでている場合には外科治療をお勧めしています。外科手術は逆流している静脈を凝固・切断することで病変を消失させます (図4I). 図4H 図4I 図4H:脊髄硬膜動静脈瘻に対する血管内治療 (経動脈的塞栓術) 太ももから細いカテーテル (マイクロカテーテル)を栄養動脈まで誘導する.そこから血管を閉塞させる液体 (液体塞栓物質)を注入して,動静脈シャントの異常血流を遮断する. 図4I:脊髄硬膜動静脈瘻に対する外科手術 背中側から背骨の一部を削ってアプローチをする.脊髄を覆う硬膜を切開して,硬膜の中から動静脈シャントの異常血流が逆流している脊髄静脈を凝固・切断することで病変は消失する. 4-4. 脊髄硬膜外動静脈瘻 脊髄硬膜外動静脈瘻は脊髄の硬膜と脊椎との間の硬膜外腔にできた動静脈瘻で (図4J),脊髄硬膜動静脈瘻と同様に中高年の男性に多く,動静脈シャントの異常血流が脊髄の静脈へ逆流して脊髄うっ血をきたすことで,両下肢の運動麻痺,感覚障害,排尿・排便障害などの症状を呈します.脊髄硬膜動静脈瘻と異なるのは病変の位置で,脊髄硬膜外動静脈瘻の多くは腰やお尻の高さにある腰椎・仙椎レベルに認められます.脊髄硬膜動静脈瘻と非常によく似た疾患ですが,脊髄硬膜外動静脈瘻は稀に動静脈シャントの血流量が非常に多い場合があり,その際には周囲の神経などを圧迫することで症状を呈します.治療は血管内治療と外科治療のいずれも可能ですが,脊髄硬膜動静脈瘻よりもさらに血管内治療に向いており,当院では血管内治療で根治を目指します (図4K). 図4J 図4K 図4J:脊髄硬膜外動静脈瘻 正常の硬膜外腔には脊髄からの静脈が流出しているため,この部位に動静脈瘻ができると動静脈シャントの異常血流が脊髄の静脈へ逆流することがある. 図4K:脊髄硬膜外動静脈瘻に対する血管内治療 (経動脈的塞栓術) 太ももから細いカテーテル (マイクロカテーテル)を栄養動脈まで誘導して,そこから血管を閉塞させる液体 (液体塞栓物質)を注入する.動静脈シャント部 (☆)を閉塞させることで,脊髄静脈への逆流は消失する. 5. 頭頚部動静脈奇形 頭皮,顔面,耳などにできた動静脈奇形で,時に動静脈瘻の形態をとることもあります.症状は病変の部位,動静脈シャントの量 (シャント血流量)によって様々ですが,動静脈シャントの血流量がそれほど多くない場合は皮膚の発赤や熱感を認め,病変部の腫脹や拍動はあまり目立ちません (静止期) (図5A).しかしシャント血流量が増えてくると,病変部は腫脹して血管の拍動を認めるようになります (拡張期) (図5B).さらに進行すると疼痛が出現し,さらに病変部の皮膚に潰瘍ができて出血するようになります (破壊期) (図5C).シャント血流量は年齢が上がるにつれて増えてくることが多く,病変部の腫脹も徐々に強くなっていきます.特に思春期では半数以上で進行を認めます.また頭頚部動静脈奇形は外傷,感染,ホルモン変化,血行動態の変化などによって急激に増大することがあり,特に妊娠によっても増悪することがあります. 図5A 図5B 図5C 図5:頬部の動静脈奇形 5A:静止期.病変部の腫脹はあまりなく,外表上は赤あざのように見える.病変部の皮膚は熱感を認める. 5B:拡張期.病変部が腫脹し,触ると動脈の拍動を認める. 5C:破壊期.病変部の色調が悪くなり,疼痛が出現する.また時に出血を認める. 治療のタイミングは疼痛,潰瘍,出血などの症状が出現している場合や美容的理由がある場合には治療適応となります.病変部の発赤や腫脹のみの場合には病変の大きさや血管構築などから根治が可能かどうかで治療適応を判断します.治療は血管内治療や外科手術(切除+再建)で行います.動静脈瘻の場合だと血管内治療単独で根治を狙うことも可能ですが,動静脈奇形は複雑な血管構築をとることが多く,そのため血管内治療と外科手術を組み合わせた集学的治療を行わなくてはいけません.当院では血管内治療は脳神経外科で,外科手術は脳神経外科と形成外科の合同で行っています.病変を根治させることが理想ではありますが,美容的な面を考慮すると実際には難しいことが多く,その場合には症状の改善やコントロールが治療目標となります.根治できない場合には血管内治療も外科的切除も病変にとっては一種の外傷であるため,それらを契機に病変が増大する危険性もあります.したがって頭頚部動静脈奇形の治療は病態をしっかりと理解している血管内治療医と外科医で行わなくてはいけません. 6. 肺動静脈瘻 (肺動静脈奇形) 肺にできた動静脈シャント疾患で肺動静脈奇形とも呼ばれますが,ほとんどが動静脈瘻の血管構築となっているので,ここでは肺動静脈瘻で統一します. 正常の肺の毛細血管の役割は圧調節だけでなく,ガス交換もあります (図6A).これは私たちが口や鼻から吸い込んだ酸素を血液中に取り込んで,代わりに二酸化炭素を血液中から回収しています.肺動静脈瘻があるとそこを流れる血液は毛細血管を通らないためガス交換が行われず (図6B),したがって血液中の酸素量は少なくなってしまいます.その結果,普段は自覚症状がなくても運動をするとすぐに息切れが生じるようになります.息切れの程度は肺動静脈瘻の大きさや数によりますが,大きな肺動静脈瘻や多発性の肺動静脈瘻の患者さんでは血液中の酸素濃度 (血中酸素飽和度)が普段から低くなります. 肺の毛細血管には他にフィルターとしての機能もあります (図6A).肺動脈には全身の臓器を巡った血液が流れますが,その中には血の塊 (血栓)や細菌が入っていることがあります.肺の毛細血管はこれらを濾しとっており,これらが心臓から全身に飛んでいかないようにしています.肺動静脈瘻では正常の毛細血管がないためフィルターが機能せず,そのため血栓や細菌が肺を通り過ぎて心臓から全身の臓器に飛んでいってしまいます (これを奇異性塞栓症と言います).特に脳へ飛んでいくことが多く,血栓が飛んでいくと脳梗塞,細菌だと脳膿瘍を起こします (図6B).脳梗塞や脳膿瘍を発症すると適切な治療を行っても運動麻痺や言語障害などの神経症状が後遺症となる危険性があり,また大きな脳梗塞や脳膿瘍では生命に危険が及ぶこともあります. 図6A 図6B 図6A:正常の肺の毛細血管 正常の肺の毛細血管は血液中の酸素と二酸化炭素のガス交換を行うだけでなく,血液中にできた小さな血栓や血液中に入った細菌が心臓を介して全身に飛んでいかないようにするフィルターの役割もある. 図6B:肺動静脈瘻 肺動静脈瘻は正常の毛細血管を持たないためガス交換が行われず,またフィルターとしての機能も持たない.そのため小さな血栓や細菌が心臓を介して全身に飛んでいく危険性がある.脳へ飛んでいくと脳梗塞や脳膿瘍を起こす. 肺動静脈瘻の治療は外科手術もありますが,現在では血管内治療 (図6C)が第一選択です.息切れなどの呼吸症状を呈している患者さんはもちろんですが,無症状の患者さんでもある程度の大きさ以上の病変であれば治療をお勧めしています.肺動静脈瘻は出血することもありますが,実際には妊娠中を除いて非常に稀ですので,無症状の患者さんの治療目的は主に脳梗塞や脳膿瘍の予防になります.逆に妊娠可能な年齢の女性の場合には,出血を予防するために妊娠前に治療を受けることをお勧めします. 図6C 図6C:肺動静脈瘻に対する血管内治療 太ももの静脈から心臓を通して細いカテーテル (マイクロカテーテル)を病変まで誘導する. 静脈瘤から栄養動脈にかけてプラチナコイルを留置して,病変を消失させる. 肺動静脈瘻はオスラー病という遺伝性疾患に合併することが多いので,肺動静脈瘻の患者さんは必ずオスラー病かどうかの診察を受ける必要があります.詳しく見る
脳神経外科動静脈シャント疾患 (動静脈奇形、動静脈瘻)1. 動静脈シャント疾患とは 血液は正常では動脈-細動脈-毛細血管-細静脈-静脈の順に流れています (図1A).一方,動静脈シャント (短絡)は動脈が毛細血管を介さずに静脈が直接つながってしまった状態です.動静脈シャントを認める血管奇形の総称を動静脈シャント疾患と言い,動静脈奇形や動静脈瘻が含まれます. 毛細血管には様々な役割がありますが,その1つに血圧の調整があります.したがって毛細血管を介さない動静脈シャント疾患では,圧の高い動脈の血流が,本来は圧の低い静脈に直接流れ込んでしまうため病変部に負担がかかり,その結果として様々な症状を引き起こします. 動静脈奇形は比較的細い動静脈レベルで動静脈シャントが形成されており,動静脈シャント部はナイダスと呼ばれる異常血管の塊となっています (図1B).一方,動静脈瘻は動静脈奇形よりも太いレベルで動静脈シャントが形成されており,多くの場合,動静脈シャント部の静脈が拡張して静脈瘤となっています (図1C).動静脈シャントができる原因は完全には解明されていませんが,遺伝子異常,炎症,外傷 (手術を含む)などが原因の1つと考えられています. 図1A 図1B 図1C 図1A:正常の血管構造 血管は動脈,細動脈,毛細血管の順にその径が小さくなり,血管にかかる圧は主に細動脈と毛細血管レベルで下がっていく.その後,細静脈,静脈の順にその径は太くなるが,血管にかかる圧は低いままである. 図1B:動静脈奇形 動静脈奇形は比較的細い動脈と静脈がナイダスと呼ばれる異常血管の塊を介して動静脈シャントを形成している. 図1C:動静脈瘻 動静脈瘻は動静脈奇形よりも太いレベルで動脈と静脈が直接つながっており,動静脈シャント部には負担がかかるため静脈瘤を形成している. 動静脈シャント疾患は病変の部位,血管の構造,血流の速さ (シャント血流量)などの個人差が非常に大きく,そのため症状や適切な治療法は患者さん毎に異なります.また頚部内頚動脈狭窄症や脳動脈瘤よりも稀な疾患で,治療もより戦略的に行う必要があり,専門性の高い疾患となります.安易に治療をすることで,その先の治療が困難になることもありますので,最初から専門施設での治療をお勧めします. 動静脈シャント疾患は脳や脊髄だけでなく顔面,手足,肺など全身のどこにでもできる可能性があります.当院では脳・脊髄に限らず全身のあらゆる動静脈シャント疾患に対して脳神経外科が対応しています.以下に代表的な動静脈シャント疾患である脳動静脈奇形,硬膜動静脈瘻,脊髄・脊椎動静脈シャント疾患,頭頚部動静脈奇形,肺動静脈瘻について解説していきます. 2. 脳動静脈奇形 脳の中にできた動静脈奇形 (図2A)で,多くは20~40歳代に脳出血で発症します.また出血以外にも頭痛やけいれんなどで発症することもあります.脳出血で発症した場合には病変の部位によって運動麻痺,言語障害などの様々な神経症状をきたし,これらは後遺症となるリスクがあります.さらに出血が大きい場合には生命が脅かされることもあります. 図2A 図2A:脳動静脈奇形の血管構造 正常の脳動脈からナイダスへの栄養動脈が分岐し,動静脈シャントの血流はナイダスから流出静脈へと向かう. ナイダス部の脳は機能していないが,その周囲の脳は機能している. 年間出血率は2%前後ですが,脳動静脈奇形は見つかれば全例で治療すべきというわけではありません.経過観察での出血リスクと治療に伴う合併症のリスクとのバランスを考えて,患者さん毎に治療方針を決定します.治療には開頭手術,定位放射線治療 (ガンマナイフ),血管内治療などがありますが,その選択は患者さんの年齢,症状,病変の大きさ,血管構築などから総合的に判断します.具体的には脳ドックなどで偶然に見つかった場合 (無症状)には,経過観察か治療を行うにしてもリスクが低い定位放射線治療 (ガンマナイフ) (図2B)となります.出血以外の症状 (頭痛やけいれん)で見つかった場合 (非出血例)は,まず症状に対する対症療法 (内科的治療)を行いますが,そちらに抵抗性の場合には治療を検討します. 図2B 図2B:脳動静脈奇形に対するガンマナイフ 約200本のガンマ線 (放射線の1種)をナイダスに集中するように照射する. 1本1本のガンマ線は弱い放射線であるので,周囲の正常脳への影響は最小限であるが,ガンマ線が集まるナイダスには強い放射線が当たることになる. ガンマナイフでは治療後に病変はすぐに消失せず,2~3年かけて徐々に閉塞していく. 出血で発症した場合 (出血例)には再出血のリスクが高まりますので,全例で治療を行います.治療に関しては血管内治療 (術前塞栓術)を併用した開頭手術 (図2C, D)をまず検討し,開頭手術のリスクが高い部位の病変に対しては定位放射線治療をお勧めしています.また出血した部位がはっきりしている場合には,先に出血した部分のみを先に血管内治療で閉塞させ,その後に次の治療を検討することもあります.脳動静脈奇形は細い動静脈レベルで動静脈シャントが形成されていますので,血管内治療のみで安全かつ確実に根治させることは困難なのが現状です. 当院では出血例にせよ非出血例にせよ,より確実にまた安全かつ低侵襲に行える治療法を選択します. 図2C 図2D 図2C:脳動静脈奇形に対する血管内治療 (術前塞栓術) 太ももまたは手首から細いカテーテル (マイクロカテーテル)を栄養動脈まで誘導し,そこから血管を閉塞させるための液体 (液体塞栓物質)を注入する.正常の動脈は閉塞させない範囲で可能な限りナイダスを閉塞させ,開頭手術の際の出血が減るようにする. 図2D:脳動静脈奇形に対する開頭手術 開頭手術では丁寧にナイダスの部分のみを切除して,ナイダス周囲の正常脳や正常の血管を損傷しないようにする. 3. 硬膜動静脈瘻 硬膜は脳と頭蓋骨の間にある硬い膜で,脳を保護しているだけでなく,その中には正常の脳静脈が脳の表面から心臓へ還るための流出路である硬膜静脈洞も存在しています (図3A, B).硬膜動静脈瘻の多くはその硬膜静脈洞の壁またはその周囲に発生します.好発年齢は中高年代で,特に目の奥 (海綿静脈洞部)や耳の後ろ(横・S状静脈洞部)が好発部位となります.硬膜には非常に多くの動脈があるため,硬膜動静脈瘻は多数の栄養動脈が関与しているのが特徴です.また病変周囲の硬膜静脈洞が閉塞していることもあり,これは硬膜動静脈瘻による症状にも関係します. 図3A 図3B 図3A:硬膜と脳,頭蓋骨との関係 (断面図) 硬膜は脳と頭蓋骨との間にあり,その中には脳の表面からの静脈を受ける硬膜静脈洞が存在する. 図3B:代表的な硬膜静脈洞 (側面から見た図) 硬膜静脈洞は様々な部位で脳からの静脈を受けており,その血流を心臓へ還している. 硬膜動静脈瘻の症状は病変の部位により様々ですが,大きくは正常の脳静脈の流出を邪魔しているかどうかで分けられます.正常の脳静脈の流出を邪魔していないもの (図3C)の多くは,頭痛や心臓の拍動に一致した耳鳴りなどで発症し,症状の程度は個人差がありますが,脳うっ血や脳出血を起こすことはありません.したがって正常の脳静脈の流出を邪魔していない硬膜動静脈瘻は,症状の程度によって治療を行うか経過観察かを決定します.症状が軽く経過観察とした場合でも,後に脳静脈の流出を邪魔するようものへと進行することがあるため,定期的なMRI検査は必須となります. 図3C 図3C:硬膜動静脈瘻 (正常の脳静脈の流出を邪魔していないタイプ) 多数の栄養動脈がシャント部 (☆)に収束している. 動静脈シャントの異常血流はそこから硬膜静脈洞を使って心臓に向かって流出している. 一方,正常の脳静脈の流出を邪魔しているものは,病変周囲の硬膜静脈洞が閉塞している場合などで認められます (図3D).このような場合では動静脈シャントの異常血流が脳静脈に逆流することがあり,そうなると正常の脳静脈の流出は邪魔され,進行すると脳はうっ血して正常に機能しなくなります.そのためけいれんや運動麻痺,言語障害などの神経症状を認め,また認知障害が急速に進行することもあります.脳うっ血を起こしていると脳出血を起こすリスクも高く,年間出血率は8-19%になります.したがって正常の脳静脈の流出を邪魔している硬膜動静脈瘻は,症状がなくても基本的に治療をお勧めしています. 図3D 図3D:硬膜動静脈瘻 (正常の脳静脈の流出を邪魔しているタイプ) 硬膜静脈洞が閉塞していることで,動静脈シャントの異常血流は心臓側へ流出することができず,脳静脈を逆流して脳内へ向かっている. 硬膜動静脈瘻の治療のほとんどは血管内治療で行い,シャント部を閉塞させます.病変の部位,血管構築に応じて,動脈側からの治療 (経動脈的塞栓術) (図3E)もしくは静脈側からの治療 (経静脈的塞栓術) (図3F)を選択します.血管構築が複雑な場合は複数回の血管内治療を要することがあり,血管内治療で病変を消失させることが困難な場合には定位放射線治療 (ガンマナイフ)を追加することもあります.また血管内治療でカテーテルが到達困難な病変や脳神経麻痺が出現するリスクが高い病変などは開頭手術をお勧めすることもあります. 図3E 図3F 図3E:硬膜動静脈瘻に対する経動脈的塞栓術 太ももまたは手首から細いカテーテル (マイクロカテーテル)をできる限り栄養動脈の奥 (動静脈シャント部の近く)に誘導し,そこから血管を閉塞させる液体 (液体塞栓物質)を注入する.病変が消失することで動静脈シャントの異常血流が逆流していた脳静脈は正常の流れに戻る. 図3F:硬膜動静脈瘻に対する経静脈的塞栓術 太ももまたは首の静脈からマイクロカテーテルを病変に関与している硬膜静脈洞まで進め,動静脈シャントの異常血流が流出している硬膜静脈洞をシャント部も含めてプラチナコイルなどで閉塞させる.病変が消失することで動静脈シャントの異常血流が逆流していた脳静脈は正常の流れに戻る. 4. 脊髄・脊椎動静脈シャント疾患 脳から腰に向かって連続している脊髄は,その周囲を脳と同様に硬膜に覆われ,さらにその外側には骨である脊椎がある.また硬膜と脊椎の間には硬膜外腔というスペースが存在しており (図4A, B),その中を脊髄や脊椎に向かう動脈,脊髄からの神経,脊髄や脊椎からの静脈が走行しています.脊髄・脊椎動静脈シャント疾患には病変の部位に応じて,脊髄髄内動静脈奇形,脊髄辺縁動静脈瘻,脊髄硬膜動静脈瘻,脊髄硬膜外動静脈瘻などがある.脊髄・脊椎動静脈シャント疾患は脳の動静脈シャント疾患と比べて頻度はさらに低く,より専門性が高くなるので,その治療は経験豊富な施設で受ける必要があります. 図4A 図4B 図4A, B:正常の脊髄,硬膜,硬膜外腔,脊椎の位置関係 (A: 前方から見た図,B: 図4Aの①レベルでの横断面) 脊髄は脊椎の真ん中にあるトンネル状の空間 (脊柱管)に首から腰に向かって認められ,その周囲は硬膜に覆われている.硬膜と脊柱管の壁との間のスペースが硬膜外腔となる. 4-1. 脊髄髄内動静脈奇形 脊髄髄内動静脈奇形は脊髄内にできた動静脈奇形 (図4C)です.脊髄は部位によって頚髄 (首の高さ),胸髄 (胸の高さ),腰髄 (腰の高さ)に分けられます.その中で脊髄髄内動静脈奇形は胸髄レベルにできることが多く,20~40歳代に出血や脊髄うっ血 (脊髄の正常静脈の流れが邪魔されて脊髄が腫れる)などで発症することが多いのが特徴です.症状は病変に部位によって異なり,胸髄と腰髄レベルでは両下肢の運動麻痺,感覚障害,排尿・排便障害をきたし,頚髄レベルではそれらに加えて両上肢の運動麻痺,感覚障害や重症の場合には呼吸障害をきたします.年間出血率は4%前後で,約30%に動脈瘤を合併します. 図4C 図4C:脊髄髄内動静脈奇形 正常の脊髄動脈から複数の栄養動脈がナイダスへ分岐しており,動静脈シャントの異常血流はナイダスから流出静脈へ向かっている. ナイダス内に出血の原因となる動脈瘤を伴うことがある. 脊髄は脳と比べて非常に小さく,そのため外科手術,血管内治療ともに脳動静脈奇形よりもリスクが高くなるため,治療は原則的に症状を呈している場合にのみ行います.外科手術は根治できる可能性があるものの,手術の際に病変の周囲にある正常の脊髄が傷ついて神経症状が悪化する可能性もあるため,当院では外科手術よりも血管内治療を優先しています.血管内治療も目標は病変の消失ではなく,出血した動脈瘤部分のみを閉塞させるか (図4D),または安全なところのみ閉塞させて動静脈シャント量を減弱させ,再出血の予防または症状の改善を狙います. 図4D 図4D:脊髄髄内動静脈奇形に対する血管内治療 (経動脈的塞栓術) 太ももから細いカテーテル (マイクロカテーテル)を栄養動脈まで誘導し,そこから血管を閉塞させる液体 (液体塞栓物質)を注入する. 出血の原因となるナイダス内の動脈瘤を閉塞させることで,再出血の危険性を下げることができる. 4-2. 脊髄辺縁動静脈瘻 脊髄表面にできた動静脈瘻 (図4E)で,胸髄レベルにでき,動静脈シャント部には静脈瘤を認めることが多いのが特徴です.好発年齢は小児から若年者で,脊髄うっ血や出血だけでなく,静脈瘤が脊髄を圧迫して症状を呈することもあります.非常に稀な疾患なので年間出血率などの詳細は分かっていません.症状に関しては脊髄髄内動静脈奇形と同様ですが,病変の血管構築によっては治療で根治が期待できることが大きく異なります.脊髄辺縁動静脈瘻は脊髄の表面に存在するため外科手術も可能ですが,当院ではより低侵襲に行うことのできる血管内治療を選択しています (図4F).症状を認めている場合は全例で治療を行いますが,症状を認めていない場合 (無症状)でも一旦症状が出現すると後遺症となる危険性が高い疾患なので,治療のリスクとのバランスを見て治療をお勧めすることもあります. 図4E 図4F 図4E:脊髄辺縁動静脈瘻 脊髄辺縁動静脈瘻は脊髄の表面に存在し,脊髄髄内動静脈奇形よりも栄養動脈が太い.また動静脈シャント部には静脈瘤を伴うことが多い. 図4F:脊髄辺縁動静脈瘻に対する血管内治療 (経動脈的塞栓術) 太ももから細いカテーテル (マイクロカテーテル)を栄養動脈まで誘導する.そこから血管を閉塞させる液体 (液体塞栓物質)を注入して,動静脈シャントの異常血流を遮断する. 4-3. 脊髄硬膜動静脈瘻 脊髄を覆う硬膜にできた動静脈瘻 (図4G)で,中高年の男性に多く認められます.背骨で言うと肋骨がつながっている胸椎レベルに多く見られ,動静脈シャントの異常血流が脊髄の静脈に逆流することで脊髄の正常静脈の流れが邪魔されて脊髄がうっ血し,両下肢の運動麻痺,感覚障害,排尿・排便障害などで発症します. 図4G 図4G:脊髄硬膜動静脈瘻 脊髄硬膜動静脈瘻は脊髄を覆う硬膜に動静脈シャントを形成している. 動静脈シャントの異常血流が脊髄の静脈へ逆流することで,正常の脊髄静脈の流れを邪魔して脊髄うっ血をきたす. 治療は血管内治療と外科手術のどちらでも可能ですが,当院ではほとんどが血管内治療で行っています (図4H).ただし閉塞させる動脈の傍から脊髄への正常の枝がでている場合には外科治療をお勧めしています。外科手術は逆流している静脈を凝固・切断することで病変を消失させます (図4I). 図4H 図4I 図4H:脊髄硬膜動静脈瘻に対する血管内治療 (経動脈的塞栓術) 太ももから細いカテーテル (マイクロカテーテル)を栄養動脈まで誘導する.そこから血管を閉塞させる液体 (液体塞栓物質)を注入して,動静脈シャントの異常血流を遮断する. 図4I:脊髄硬膜動静脈瘻に対する外科手術 背中側から背骨の一部を削ってアプローチをする.脊髄を覆う硬膜を切開して,硬膜の中から動静脈シャントの異常血流が逆流している脊髄静脈を凝固・切断することで病変は消失する. 4-4. 脊髄硬膜外動静脈瘻 脊髄硬膜外動静脈瘻は脊髄の硬膜と脊椎との間の硬膜外腔にできた動静脈瘻で (図4J),脊髄硬膜動静脈瘻と同様に中高年の男性に多く,動静脈シャントの異常血流が脊髄の静脈へ逆流して脊髄うっ血をきたすことで,両下肢の運動麻痺,感覚障害,排尿・排便障害などの症状を呈します.脊髄硬膜動静脈瘻と異なるのは病変の位置で,脊髄硬膜外動静脈瘻の多くは腰やお尻の高さにある腰椎・仙椎レベルに認められます.脊髄硬膜動静脈瘻と非常によく似た疾患ですが,脊髄硬膜外動静脈瘻は稀に動静脈シャントの血流量が非常に多い場合があり,その際には周囲の神経などを圧迫することで症状を呈します.治療は血管内治療と外科治療のいずれも可能ですが,脊髄硬膜動静脈瘻よりもさらに血管内治療に向いており,当院では血管内治療で根治を目指します (図4K). 図4J 図4K 図4J:脊髄硬膜外動静脈瘻 正常の硬膜外腔には脊髄からの静脈が流出しているため,この部位に動静脈瘻ができると動静脈シャントの異常血流が脊髄の静脈へ逆流することがある. 図4K:脊髄硬膜外動静脈瘻に対する血管内治療 (経動脈的塞栓術) 太ももから細いカテーテル (マイクロカテーテル)を栄養動脈まで誘導して,そこから血管を閉塞させる液体 (液体塞栓物質)を注入する.動静脈シャント部 (☆)を閉塞させることで,脊髄静脈への逆流は消失する. 5. 頭頚部動静脈奇形 頭皮,顔面,耳などにできた動静脈奇形で,時に動静脈瘻の形態をとることもあります.症状は病変の部位,動静脈シャントの量 (シャント血流量)によって様々ですが,動静脈シャントの血流量がそれほど多くない場合は皮膚の発赤や熱感を認め,病変部の腫脹や拍動はあまり目立ちません (静止期) (図5A).しかしシャント血流量が増えてくると,病変部は腫脹して血管の拍動を認めるようになります (拡張期) (図5B).さらに進行すると疼痛が出現し,さらに病変部の皮膚に潰瘍ができて出血するようになります (破壊期) (図5C).シャント血流量は年齢が上がるにつれて増えてくることが多く,病変部の腫脹も徐々に強くなっていきます.特に思春期では半数以上で進行を認めます.また頭頚部動静脈奇形は外傷,感染,ホルモン変化,血行動態の変化などによって急激に増大することがあり,特に妊娠によっても増悪することがあります. 図5A 図5B 図5C 図5:頬部の動静脈奇形 5A:静止期.病変部の腫脹はあまりなく,外表上は赤あざのように見える.病変部の皮膚は熱感を認める. 5B:拡張期.病変部が腫脹し,触ると動脈の拍動を認める. 5C:破壊期.病変部の色調が悪くなり,疼痛が出現する.また時に出血を認める. 治療のタイミングは疼痛,潰瘍,出血などの症状が出現している場合や美容的理由がある場合には治療適応となります.病変部の発赤や腫脹のみの場合には病変の大きさや血管構築などから根治が可能かどうかで治療適応を判断します.治療は血管内治療や外科手術(切除+再建)で行います.動静脈瘻の場合だと血管内治療単独で根治を狙うことも可能ですが,動静脈奇形は複雑な血管構築をとることが多く,そのため血管内治療と外科手術を組み合わせた集学的治療を行わなくてはいけません.当院では血管内治療は脳神経外科で,外科手術は脳神経外科と形成外科の合同で行っています.病変を根治させることが理想ではありますが,美容的な面を考慮すると実際には難しいことが多く,その場合には症状の改善やコントロールが治療目標となります.根治できない場合には血管内治療も外科的切除も病変にとっては一種の外傷であるため,それらを契機に病変が増大する危険性もあります.したがって頭頚部動静脈奇形の治療は病態をしっかりと理解している血管内治療医と外科医で行わなくてはいけません. 6. 肺動静脈瘻 (肺動静脈奇形) 肺にできた動静脈シャント疾患で肺動静脈奇形とも呼ばれますが,ほとんどが動静脈瘻の血管構築となっているので,ここでは肺動静脈瘻で統一します. 正常の肺の毛細血管の役割は圧調節だけでなく,ガス交換もあります (図6A).これは私たちが口や鼻から吸い込んだ酸素を血液中に取り込んで,代わりに二酸化炭素を血液中から回収しています.肺動静脈瘻があるとそこを流れる血液は毛細血管を通らないためガス交換が行われず (図6B),したがって血液中の酸素量は少なくなってしまいます.その結果,普段は自覚症状がなくても運動をするとすぐに息切れが生じるようになります.息切れの程度は肺動静脈瘻の大きさや数によりますが,大きな肺動静脈瘻や多発性の肺動静脈瘻の患者さんでは血液中の酸素濃度 (血中酸素飽和度)が普段から低くなります. 肺の毛細血管には他にフィルターとしての機能もあります (図6A).肺動脈には全身の臓器を巡った血液が流れますが,その中には血の塊 (血栓)や細菌が入っていることがあります.肺の毛細血管はこれらを濾しとっており,これらが心臓から全身に飛んでいかないようにしています.肺動静脈瘻では正常の毛細血管がないためフィルターが機能せず,そのため血栓や細菌が肺を通り過ぎて心臓から全身の臓器に飛んでいってしまいます (これを奇異性塞栓症と言います).特に脳へ飛んでいくことが多く,血栓が飛んでいくと脳梗塞,細菌だと脳膿瘍を起こします (図6B).脳梗塞や脳膿瘍を発症すると適切な治療を行っても運動麻痺や言語障害などの神経症状が後遺症となる危険性があり,また大きな脳梗塞や脳膿瘍では生命に危険が及ぶこともあります. 図6A 図6B 図6A:正常の肺の毛細血管 正常の肺の毛細血管は血液中の酸素と二酸化炭素のガス交換を行うだけでなく,血液中にできた小さな血栓や血液中に入った細菌が心臓を介して全身に飛んでいかないようにするフィルターの役割もある. 図6B:肺動静脈瘻 肺動静脈瘻は正常の毛細血管を持たないためガス交換が行われず,またフィルターとしての機能も持たない.そのため小さな血栓や細菌が心臓を介して全身に飛んでいく危険性がある.脳へ飛んでいくと脳梗塞や脳膿瘍を起こす. 肺動静脈瘻の治療は外科手術もありますが,現在では血管内治療 (図6C)が第一選択です.息切れなどの呼吸症状を呈している患者さんはもちろんですが,無症状の患者さんでもある程度の大きさ以上の病変であれば治療をお勧めしています.肺動静脈瘻は出血することもありますが,実際には妊娠中を除いて非常に稀ですので,無症状の患者さんの治療目的は主に脳梗塞や脳膿瘍の予防になります.逆に妊娠可能な年齢の女性の場合には,出血を予防するために妊娠前に治療を受けることをお勧めします. 図6C 図6C:肺動静脈瘻に対する血管内治療 太ももの静脈から心臓を通して細いカテーテル (マイクロカテーテル)を病変まで誘導する. 静脈瘤から栄養動脈にかけてプラチナコイルを留置して,病変を消失させる. 肺動静脈瘻はオスラー病という遺伝性疾患に合併することが多いので,肺動静脈瘻の患者さんは必ずオスラー病かどうかの診察を受ける必要があります.詳しく見る -
 脳神経外科小児脳神経外科小児頭蓋内動静脈シャント疾患 (ガレン大静脈瘤,硬膜静脈洞奇形,乳幼児型硬膜動静脈瘻,脳動静脈瘻)動静脈シャント疾患とは動脈が毛細血管を介さずに静脈につながってしまった血管奇形です.詳しくは動静脈シャント疾患とはを参照して下さい. 小児の頭蓋内動静脈シャント疾患は成人と比べると非常に稀であるためより専門性が高く,その診断・治療は経験豊富な施設で受ける必要があります.ガレン大静脈瘤,硬膜静脈洞奇形,乳幼児型硬膜動静脈瘻,脳動静脈瘻,脳動静脈奇形が含まれ,病変の部位や血管構築などはそれぞれで異なっていますが,その症状は種類に関係なく発症する時期によってほぼ共通しています.例えばお母さんのお腹の中にいる時期から新生児期 (生後28日まで)までは動静脈シャントの血流が心臓に負担をかけて心不全を呈します.新生児期以降から2歳までの乳幼児期は動静脈シャントの血流が正常の脳静脈の流れを邪魔することで頭位拡大や水頭症などを呈し,乳幼児期以降は成人と同様に頭痛,けいれん,神経症状などで発症します. 以下にそれぞれの疾患について解説します. 1. ガレン大静脈瘤 ガレン大静脈瘤は脳の中心にあるガレン大静脈という部位にできた動静脈シャント疾患です.子供がお母さんのお腹の中にいる時期にできるため,動静脈シャントの血流量が多い場合には産まれる前から心不全を呈することもあります.また出産時はそれほど問題なくても,産まれてから数日の間に心不全が悪化することもあります.逆にシャント血流量がそれほど多くない場合には,乳幼児期までに頭位拡大や水頭症で発症します. 治療は血管内治療で,動脈側から動静脈シャント部を閉塞させます.新生児期に発症するガレン大静脈瘤は血管構築が複雑なタイプ (図1A)で,そのため複数回の治療を要します.それに比べて乳幼児期に発症するものは血管構築がシンプルなタイプ (図1B)が多いので,1-2回の治療で完全閉塞が期待できます. 図1A 図1B 図1:ガレン大静脈瘤 (側面から見た図) 1A:血管構築が複雑なタイプ.多数の栄養動脈が静脈瘤の様々な箇所で動静脈シャントを形成している (☆).新生児期に心不全で発症することが多い. 1B:血管構築がシンプルなタイプ.動静脈シャント部 (☆)は1~数か所と少なく,乳幼児期に頭位拡大や水頭症で発症することが多い. ガレン大静脈瘤は基礎疾患として毛細血管奇形-動静脈奇形を伴っていることがあり,これは遺伝性疾患であるため両親への問診・診察も必要となります. 2. 硬膜静脈洞奇形 硬膜静脈洞奇形は子供がお母さんのお腹の中にいる時期に,後頭部の硬膜静脈洞 (静脈洞交会,横静脈洞)が異常拡張して動静脈シャントが形成されたものです (図2A, B).多数の栄養動脈が異常拡張した硬膜静脈洞の壁の様々な部位で動静脈シャントを形成していることが多く認められます.ガレン大静脈瘤と同様に産まれる前から産まれてから数日の間は心不全を呈し,その後の乳幼児期では頭位拡大や水頭症で発症します. 治療は血管内治療で,1-数回の治療を要します.多くの場合で動脈側からの治療が中心で,状況に応じて静脈側からの治療も行います. 図2A 図2B 図2A:後頭部の正常の硬膜静脈洞 (正面から見た図) 後頭部の硬膜静脈洞は静脈洞交会,横静脈洞,S状静脈洞などがある.頭頂部からくる上矢状洞が後頭部正中の静脈洞交会で左右の横静脈洞に分かれる.左右の横静脈洞はそれぞれS状静脈洞となり,そこから頚部の静脈へつながる. 図2B:硬膜静脈洞奇形 多数の栄養動脈が異常拡張した硬膜静脈洞の壁に様々な部位で動静脈シャントを形成している (☆). 3. 乳幼児型硬膜動静脈瘻 乳児型硬膜動静脈瘻は小児のどの年齢層でも認められますが,特に乳幼児期に多い硬膜動静脈瘻です.成人の硬膜動静脈瘻とは異なり多発性のことが多く,また経過で新たな硬膜動静脈瘻が形成されることがあることも特徴です.また病変周囲の硬膜静脈洞の閉塞を伴うことも多く,そのため動静脈シャントの異常血流が脳静脈へ逆流し,脳うっ血や脳出血を起こす危険性もあります.病態に関する詳細は成人の硬膜動静脈瘻もご参照ください. 治療は血管内治療で,動脈側と静脈側からを組み合わせて行います.血管内治療の方法は成人と大差ありませんが,成人の硬膜動静脈瘻とは異なり多発性であること,病変周囲の硬膜静脈洞の閉塞を伴うことが多いこと,また治療経過で新たな硬膜動静脈瘻が形成されることがあるなどから,治療の難易度は高く,ほとんどで複数回の治療を要します. 4. 脳動静脈瘻 脳動静脈瘻は脳動静脈奇形よりも太い動脈と静脈のレベルで動静脈シャントが形成されており,動静脈シャント部の静脈が拡張して静脈瘤となっていることが多いのが特徴です (図4A).新生児期は複雑な血管構築を呈することが多く,年齢が高くなるほど栄養動脈が1本であるシンプルな血管構築のものが多くなります.新生児期を含めて小児のどの年齢層でも認められますが,年齢が高くなるほど出血発症が多くなります. 図4A 図4A:脳動静脈瘻 太い栄養動脈が流出静脈に直接つながっている.動静脈シャント部 (☆)の静脈は拡張して静脈瘤となっていることが多い. 治療は表在性のものは外科手術も可能ですが,血管内治療が第一選択で,動脈側から動静脈シャント部を閉塞させます.閉塞させるのに使うものは液体塞栓物質 (図4B)とプラチナコイル (図4C)とがありますが,病変の血管構築に応じて使い分けます.シンプルな血管構築の場合は1回の治療で完全閉塞が期待できますが,複雑なものでは複数回の治療を要します. 図4B 図4C 図4B:脳動静脈瘻に対する血管内治療 (液体塞栓物質を用いるもの) 太ももから細いカテーテル (マイクロカテーテル)をできる限り栄養動脈の奥 (動静脈シャント部の近く)まで誘導し,そこから血管を閉塞させる液体 (液体塞栓物質)を注入する. 図4C:脳動静脈瘻に対する血管内治療 (プラチナコイルを用いるもの) 太ももから細いカテーテル (マイクロカテーテル)を栄養動脈まで進め,最終的に動静脈シャント部を超えて静脈瘤内まで誘導する.そこから栄養動脈にかけてプラチナコイルを留置する. 脳動静脈瘻は基礎疾患として遺伝性疾患であるオスラー病や毛細血管奇形-動静脈奇形を伴っていることがあるため,両親への問診・診察も必要となります. 5. 脳動静脈奇形 脳動静脈奇形の多くは成人で発症し,小児の脳静脈奇形の割合は全体の20%以下です.小児でも新生児期や乳幼児期に発症することは稀で,ほとんどが3歳以降に発症します.成人よりも脳出血で発症することが多く,また病変 (ナイダス)が大きいことが多いのも特徴です. 治療に関しては成人と大きな違いはありませんので,成人の脳動静脈奇形を参照して下さい.詳しく見る
脳神経外科小児脳神経外科小児頭蓋内動静脈シャント疾患 (ガレン大静脈瘤,硬膜静脈洞奇形,乳幼児型硬膜動静脈瘻,脳動静脈瘻)動静脈シャント疾患とは動脈が毛細血管を介さずに静脈につながってしまった血管奇形です.詳しくは動静脈シャント疾患とはを参照して下さい. 小児の頭蓋内動静脈シャント疾患は成人と比べると非常に稀であるためより専門性が高く,その診断・治療は経験豊富な施設で受ける必要があります.ガレン大静脈瘤,硬膜静脈洞奇形,乳幼児型硬膜動静脈瘻,脳動静脈瘻,脳動静脈奇形が含まれ,病変の部位や血管構築などはそれぞれで異なっていますが,その症状は種類に関係なく発症する時期によってほぼ共通しています.例えばお母さんのお腹の中にいる時期から新生児期 (生後28日まで)までは動静脈シャントの血流が心臓に負担をかけて心不全を呈します.新生児期以降から2歳までの乳幼児期は動静脈シャントの血流が正常の脳静脈の流れを邪魔することで頭位拡大や水頭症などを呈し,乳幼児期以降は成人と同様に頭痛,けいれん,神経症状などで発症します. 以下にそれぞれの疾患について解説します. 1. ガレン大静脈瘤 ガレン大静脈瘤は脳の中心にあるガレン大静脈という部位にできた動静脈シャント疾患です.子供がお母さんのお腹の中にいる時期にできるため,動静脈シャントの血流量が多い場合には産まれる前から心不全を呈することもあります.また出産時はそれほど問題なくても,産まれてから数日の間に心不全が悪化することもあります.逆にシャント血流量がそれほど多くない場合には,乳幼児期までに頭位拡大や水頭症で発症します. 治療は血管内治療で,動脈側から動静脈シャント部を閉塞させます.新生児期に発症するガレン大静脈瘤は血管構築が複雑なタイプ (図1A)で,そのため複数回の治療を要します.それに比べて乳幼児期に発症するものは血管構築がシンプルなタイプ (図1B)が多いので,1-2回の治療で完全閉塞が期待できます. 図1A 図1B 図1:ガレン大静脈瘤 (側面から見た図) 1A:血管構築が複雑なタイプ.多数の栄養動脈が静脈瘤の様々な箇所で動静脈シャントを形成している (☆).新生児期に心不全で発症することが多い. 1B:血管構築がシンプルなタイプ.動静脈シャント部 (☆)は1~数か所と少なく,乳幼児期に頭位拡大や水頭症で発症することが多い. ガレン大静脈瘤は基礎疾患として毛細血管奇形-動静脈奇形を伴っていることがあり,これは遺伝性疾患であるため両親への問診・診察も必要となります. 2. 硬膜静脈洞奇形 硬膜静脈洞奇形は子供がお母さんのお腹の中にいる時期に,後頭部の硬膜静脈洞 (静脈洞交会,横静脈洞)が異常拡張して動静脈シャントが形成されたものです (図2A, B).多数の栄養動脈が異常拡張した硬膜静脈洞の壁の様々な部位で動静脈シャントを形成していることが多く認められます.ガレン大静脈瘤と同様に産まれる前から産まれてから数日の間は心不全を呈し,その後の乳幼児期では頭位拡大や水頭症で発症します. 治療は血管内治療で,1-数回の治療を要します.多くの場合で動脈側からの治療が中心で,状況に応じて静脈側からの治療も行います. 図2A 図2B 図2A:後頭部の正常の硬膜静脈洞 (正面から見た図) 後頭部の硬膜静脈洞は静脈洞交会,横静脈洞,S状静脈洞などがある.頭頂部からくる上矢状洞が後頭部正中の静脈洞交会で左右の横静脈洞に分かれる.左右の横静脈洞はそれぞれS状静脈洞となり,そこから頚部の静脈へつながる. 図2B:硬膜静脈洞奇形 多数の栄養動脈が異常拡張した硬膜静脈洞の壁に様々な部位で動静脈シャントを形成している (☆). 3. 乳幼児型硬膜動静脈瘻 乳児型硬膜動静脈瘻は小児のどの年齢層でも認められますが,特に乳幼児期に多い硬膜動静脈瘻です.成人の硬膜動静脈瘻とは異なり多発性のことが多く,また経過で新たな硬膜動静脈瘻が形成されることがあることも特徴です.また病変周囲の硬膜静脈洞の閉塞を伴うことも多く,そのため動静脈シャントの異常血流が脳静脈へ逆流し,脳うっ血や脳出血を起こす危険性もあります.病態に関する詳細は成人の硬膜動静脈瘻もご参照ください. 治療は血管内治療で,動脈側と静脈側からを組み合わせて行います.血管内治療の方法は成人と大差ありませんが,成人の硬膜動静脈瘻とは異なり多発性であること,病変周囲の硬膜静脈洞の閉塞を伴うことが多いこと,また治療経過で新たな硬膜動静脈瘻が形成されることがあるなどから,治療の難易度は高く,ほとんどで複数回の治療を要します. 4. 脳動静脈瘻 脳動静脈瘻は脳動静脈奇形よりも太い動脈と静脈のレベルで動静脈シャントが形成されており,動静脈シャント部の静脈が拡張して静脈瘤となっていることが多いのが特徴です (図4A).新生児期は複雑な血管構築を呈することが多く,年齢が高くなるほど栄養動脈が1本であるシンプルな血管構築のものが多くなります.新生児期を含めて小児のどの年齢層でも認められますが,年齢が高くなるほど出血発症が多くなります. 図4A 図4A:脳動静脈瘻 太い栄養動脈が流出静脈に直接つながっている.動静脈シャント部 (☆)の静脈は拡張して静脈瘤となっていることが多い. 治療は表在性のものは外科手術も可能ですが,血管内治療が第一選択で,動脈側から動静脈シャント部を閉塞させます.閉塞させるのに使うものは液体塞栓物質 (図4B)とプラチナコイル (図4C)とがありますが,病変の血管構築に応じて使い分けます.シンプルな血管構築の場合は1回の治療で完全閉塞が期待できますが,複雑なものでは複数回の治療を要します. 図4B 図4C 図4B:脳動静脈瘻に対する血管内治療 (液体塞栓物質を用いるもの) 太ももから細いカテーテル (マイクロカテーテル)をできる限り栄養動脈の奥 (動静脈シャント部の近く)まで誘導し,そこから血管を閉塞させる液体 (液体塞栓物質)を注入する. 図4C:脳動静脈瘻に対する血管内治療 (プラチナコイルを用いるもの) 太ももから細いカテーテル (マイクロカテーテル)を栄養動脈まで進め,最終的に動静脈シャント部を超えて静脈瘤内まで誘導する.そこから栄養動脈にかけてプラチナコイルを留置する. 脳動静脈瘻は基礎疾患として遺伝性疾患であるオスラー病や毛細血管奇形-動静脈奇形を伴っていることがあるため,両親への問診・診察も必要となります. 5. 脳動静脈奇形 脳動静脈奇形の多くは成人で発症し,小児の脳静脈奇形の割合は全体の20%以下です.小児でも新生児期や乳幼児期に発症することは稀で,ほとんどが3歳以降に発症します.成人よりも脳出血で発症することが多く,また病変 (ナイダス)が大きいことが多いのも特徴です. 治療に関しては成人と大きな違いはありませんので,成人の脳動静脈奇形を参照して下さい.詳しく見る
WEB予約はこちら